 Se denomina smog fotoquímico a la contaminación del aire, principalmente en áreas urbanas, por originado por reacciones fotoquímicas, y otros compuestos. Como resultado se observa una atmósfera de un color marrón rojizo. El ozono es un compuesto oxidante y tóxico que puede provocar en el ser humano problemas respiratorios.
Se denomina smog fotoquímico a la contaminación del aire, principalmente en áreas urbanas, por originado por reacciones fotoquímicas, y otros compuestos. Como resultado se observa una atmósfera de un color marrón rojizo. El ozono es un compuesto oxidante y tóxico que puede provocar en el ser humano problemas respiratorios.
Este tipo de smog se describió por primera vez en LOS ANGELES en los años 40, y se suele dar en ciudades con bastante tráfico , cálidas y soleadas, y con poco movimiento de masas de aire.
Formación del smog fotoquímico
Contaminantes
Los principales contaminantes primarios son los óxidos de nitrógeno(NOx) y los compuestos orgánicos volátiles. El monóxido de nitrógeno (u óxido nítrico) se forma cuando el oxígeno y el nitrógeno atmosféricos reaccionan a altas temperaturas -esta reacción se da, por ejemplo, en los motores de combustión de los automóviles de la siguiente forma. Entre los compuestos orgánicos volátiles (COVs) se encuentran los hidrocarburos no quemados que pueden ser emitidos también por vehículos, así como disolventes o combustibles que se pueden evaporar fácilmente. También éstos pueden provenir de zonas arbóreas, al emitirse de forma natural hidrocarburos, principalmente isopreno, pineno y limoneno. Los contaminantes secundarios, formados a partir de los anteriores, a través de una serie compleja de reacciones propiciadas por la radiación solar, son el ozono, el HNO3, el nitrato de peroxialo (PAN) y otros compuestos. Reducción del smog fotoquímico Para reducir la formación de smog fotoquímico es necesario disminuir la emisión de los NOx y los COVs. Las cantidades de hidrocarburos volátiles en la atmósfera son bastante grandes comparadas con las de NOx, por lo que suelen estar en exceso. De esta forma, una reducción de éstos conduce a una disminución del smog fotoquímico menor de la esperada. Además, los hidrocarburos emitidos de forma natural pueden ser suficientes para que siga produciéndose smog (aunque en áreas urbanas no suelen ser éstos los más importantes). En cualquier caso, sigue siendo importante la reducción de los niveles de estos hidrocarburos volátiles en la atmósfera. Una de las mayores fuentes de NOx la constituyen los vehiculos. La disminución de las emisiones de óxidos de nitrógeno se hace empleando catalizadores de tres vias (los de dos vías no tratan estos gases) que los reducen a nitrogeno y oxigenos moleculares. Estos catalizadores, en el caso de los motores de gasolina, tienen una efectividad de entre un 80% a un 90%, pero sólo cuando están calientes. Además, el catalizador se va desgastando y con el tiempo va siendo menos efectivo. En el caso de los motores de diesel, la efectividad es menor. Otra de las principales fuentes de NOx es la emisión de las centrales electricas . También se pueden disminuir los NOx mediante procesos de reduccion, aunque hay otros métodos como por ejemplo llevando a cabo la combustión en varias etapas o disminuir la temperatura de la llama
Entre los compuestos orgánicos volátiles (COVs) se encuentran los hidrocarburos no quemados que pueden ser emitidos también por vehículos, así como disolventes o combustibles que se pueden evaporar fácilmente. También éstos pueden provenir de zonas arbóreas, al emitirse de forma natural hidrocarburos, principalmente isopreno, pineno y limoneno. Los contaminantes secundarios, formados a partir de los anteriores, a través de una serie compleja de reacciones propiciadas por la radiación solar, son el ozono, el HNO3, el nitrato de peroxialo (PAN) y otros compuestos. Reducción del smog fotoquímico Para reducir la formación de smog fotoquímico es necesario disminuir la emisión de los NOx y los COVs. Las cantidades de hidrocarburos volátiles en la atmósfera son bastante grandes comparadas con las de NOx, por lo que suelen estar en exceso. De esta forma, una reducción de éstos conduce a una disminución del smog fotoquímico menor de la esperada. Además, los hidrocarburos emitidos de forma natural pueden ser suficientes para que siga produciéndose smog (aunque en áreas urbanas no suelen ser éstos los más importantes). En cualquier caso, sigue siendo importante la reducción de los niveles de estos hidrocarburos volátiles en la atmósfera. Una de las mayores fuentes de NOx la constituyen los vehiculos. La disminución de las emisiones de óxidos de nitrógeno se hace empleando catalizadores de tres vias (los de dos vías no tratan estos gases) que los reducen a nitrogeno y oxigenos moleculares. Estos catalizadores, en el caso de los motores de gasolina, tienen una efectividad de entre un 80% a un 90%, pero sólo cuando están calientes. Además, el catalizador se va desgastando y con el tiempo va siendo menos efectivo. En el caso de los motores de diesel, la efectividad es menor. Otra de las principales fuentes de NOx es la emisión de las centrales electricas . También se pueden disminuir los NOx mediante procesos de reduccion, aunque hay otros métodos como por ejemplo llevando a cabo la combustión en varias etapas o disminuir la temperatura de la llamaEl smog fotoquímico es una mezcla de agentes contaminantes que incluye partículas, óxidos de nitrógeno, ozono, aldehinos, nitrato de peroxyethanoyl, hidrocarburos no activados, etc. El smog tiene a menudo una apariencia marrón debido a la presencia del dióxido del nitrógeno. Provoca dolor en los ojos. Las condiciones necesarias para la formación del smog se encuentra presente en las ciudades modernas: incluyen la luz del sol, los hidrocarburos, los óxidos de nitrógeno y las partículas que actúan como catalizador. El 9 de diciembre de 1952, se desarrollaron condiciones de bruma sobre Londres. Hací mucho frío, la mayoría de las casas quemaban leña, con carbón como el combustible principal. El humo de estos fuegos mezclados con la niebla no podía dispersarse, dando por resultado un smog que persistió por 4 días. El pH del aire durante el gran smog de Londres era tan bajo como 1,6. Durante este período murieron unas 4000 gentes más de lo esperado en esta época del año. La mayoría de estas muertes adicionales eran debido a las desórdenes respiratorias.

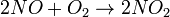

No hay comentarios:
Publicar un comentario